【题目】下图是实验室常用的装置。请据图回答:
(1)写出仪器①的名称______。收集某气体只能用E装置,可推测该气体具有的性质是_________ 。
(2)实验室用加热高锰酸钾的方法制取氧气的发生装置是____(填选项),反应的化学方程式________。
(3)实验室制取二氧化碳的发生和收集装置是_______,(填选项)CO2气体中常含有的杂质是_______。为了得到纯净、干燥的气体,除杂装置的导管气流方向连接顺序是________(填选项)。
A.a→b→c→d | B.b→a→c→d | C.c→d→a→b | D.d→c→b→a |
(4)除杂过程中发生反应的化学方程式为________________________。
参考答案:
【答案】 长颈漏斗 密度比空气小且能溶于水 B 2KMnO4 加热K2MnO4+ MnO2+O2↑ AD 氯化氢气体和水蒸气 C NaHCO3+HCl=NaCl+ H2O + CO2↑
【解析】(1)要熟悉各种仪器的名称、用途和使用方法;根据收集气体的方法可以判断气体的性质;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,二氧化碳密度比空气大,能溶于水。稀盐酸易挥发出氯化氢气体且生成的二氧化碳气体带有水蒸气;饱和碳酸氢钠溶液能和氯化氢反应生成氯化银沉淀和硝酸;浓硫酸具有吸水性,可以用来干燥二氧化碳、氢气、氧气等气体;
(4)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式。
解:(1)①的名称是长颈漏斗;收集某气体只能采用E装置,由此推测该气体密度比空气小且能溶于水。
(2)用高锰酸钾固体正确氧气需要加热,应该用B装置作为发生装置;反应的化学方程式:2KMnO4△ K2MnO4+MnO2+O2↑;
(3)实验室制取二氧化碳的发生和收集装置是AD;CO2气体中常含有的杂质是:氯化氢气体和水蒸气;为了得到纯净、干燥的CO2气体,除杂装置的导管气流方向连接顺序是:气体通过c导管进入饱和碳酸氢钠溶液中,氯化氢和饱和碳酸氢钠溶液反应,从而除去氯化氢气体,含有水蒸气的二氧化碳从d导管导出后,通过a导管进入浓硫酸中,浓硫酸能够吸收水蒸气,干燥的二氧化碳气体从b导管导出后,利用D装置收集。故填:C;
(4)在盛有硝酸银溶液的洗气瓶中发生的反应是硝酸银和氯化氢反应生成氯化银和硝酸,反应的化学方程式为:NaHCO3+HCl=NaCl+ H2O + CO2↑。
-
科目: 来源: 题型:
查看答案和解析>>【题目】有一包固体,可能由硝酸铜、硫酸钠、氯化钠、碳酸氢钠、氢氧化钠中的一种或几种组成.为了探究该固体的组成,某化学小组设计并开展以下实验:
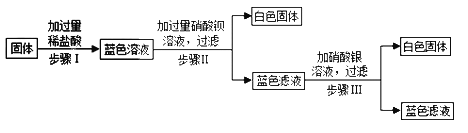
已知,步骤Ⅰ中固体全部消失,溶液呈蓝色.有气泡产生.步骤Ⅱ、Ⅲ中均可观察到有白色沉淀生成.请回答下列问题:
(1)原固体中一定含有的物质是_______________.依据是_________________.
(2)步骤II中产生白色沉淀的化学方程式是_____________________________.
(3)步骤Ⅲ所得蓝色滤液中一定含有的溶质是____________________________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
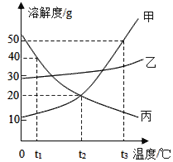
(1)在t1℃时,甲、乙、丙三种物质的溶解度由小到大的顺序为_______。
(2)在t3℃时,等质量的甲、乙、丙三种物质的饱和溶液中,溶剂质量最小的是______。
(3)降温结晶过程中,甲、乙两物质的溶解度都________(填“增大”、“减小”或“不变”)
(4)若将接近饱和的丙溶液在保持溶质的质量不变的情况下变成饱和溶液的方法是________。
(5)在t1℃时,将三种物质饱和溶液升温至t2℃时溶质的质量分数由大到小顺序是________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列粒子结构示意图,回答问题:
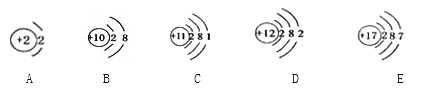
(1)具有相似化学性质的粒子______(填序号,下同)。
(2)在化学反应中易生成阳离子的是______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】属于化学变化的是
A、酒精挥发 B、冰雪融化 C、食物腐败 D、雕刻印章
-
科目: 来源: 题型:
查看答案和解析>>【题目】观察颜色是化学实验关注的重点。下列物质与水充分混合后形成无色溶液的一组是
A. Ba(OH)2、CuCl2、NaCl B. HNO3、Fe2(SO4)3、BaCl2
C. NaNO3、HC1、Al2(SO4)3 D. KMnO4、Na2CO3、 Na2SO4
-
科目: 来源: 题型:
查看答案和解析>>【题目】取氯酸钾和二氧化锰的混合物26g,加热至混合物固体质量不再减少为止,冷却后称得剩余固体质量为16 .4g,将剩余固体加入一定量的水中,充分搅拌后过滤,滤液是10%的氯化钾溶液(假设溶液无损失)。计算:
(1)反应中生成氧气的质量;(2)最后氯化钾溶液中水的质量。
相关试题

