【题目】实验室常利用下列仪器进行气体的制取和性质实验,请回答:
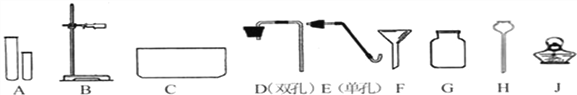
(1)写出仪器名称,H___________。
(2)实验室用高锰酸钾制取并收集纯净的氧气,应选择的仪器是________(填序号),反应的化学方程式是_______________。
(3)实验室要制取较多量的二氧化碳,装配气体发生装置时,应选择的仪器是_______(填序号)。小明同学把制取二氧化碳结束后的废液未经处理直接倒入下水道,可能造成的危害是 _______ (写一条)。
(4)利用下图装置进行实验(两玻璃管内径相同),实验前K1、K2、K3均已关闭。
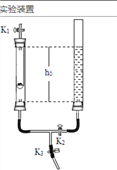
①左管燃烧匙装有足量的锌粒,右管盛有稀硫酸,打开K1、K2反应发生,方程式是_______________________,该装置的优点是________________,为使反应停止,操作是__________________。
②左管燃烧匙装有足量的白磷,右管盛水,光照引燃白磷,待白磷熄灭,冷却后,打开K2,右管液面下降,原因是______________________,至液面不在下降,右管液面高度为h1,计算空气中氧气体积分数的表达式为___________(用h0、h1表示)
参考答案:
【答案】 长颈漏斗 ABCEGJ 2KMnO4![]() K2MnO4+ MnO2+ O2↑ DGH 腐蚀铁质下水管道或污染水源等 Zn+ H2SO4 = ZnSO4 +H2↑ 控制反应的发生和停止 关闭K1 白磷消耗氧气,玻璃管内压强减少 (h0-h1)/h0×100%
K2MnO4+ MnO2+ O2↑ DGH 腐蚀铁质下水管道或污染水源等 Zn+ H2SO4 = ZnSO4 +H2↑ 控制反应的发生和停止 关闭K1 白磷消耗氧气,玻璃管内压强减少 (h0-h1)/h0×100%
【解析】(1)仪器H名称是长颈漏斗。(2)实验室用高锰酸钾制取并收集纯净的氧气,应选择的仪器是ABCEGJ,反应物是固体需加热制取气体,氧气不易溶于水,可以用排水法收集。反应的化学方程式是2KMnO4![]() K2MnO4+ MnO2+ O2↑。(3)实验室要制取较多量的二氧化碳,装配气体发生装置时,应选择的仪器是DGH,可以随时添加药品。把制取二氧化碳结束后的废液未经处理直接倒入下水道,可能造成的危害是腐蚀铁质下水管道或污染水源等,不可随意排放。(4) 利用下图装置进行实验。①左管燃烧匙装有足量的锌粒,右管盛有稀硫酸,打开K1、K2反应发生,方程式是Zn+ H2SO4 = ZnSO4 +H2↑,该装置的优点是控制反应的发生和停止。为使反应停止,操作是关闭K1,容器内气压增大,使两药品分离,反应停止。②左管燃烧匙装有足量的白磷,右管盛水,光照引燃白磷,待白磷熄灭,冷却后,打开K2,右管液面下降,原因是白磷消耗氧气,玻璃管内压强减少。至液面不在下降,右管液面高度为h1,计算空气中氧气体积分数的表达式为(h0-h1)/h0 ×100%。
K2MnO4+ MnO2+ O2↑。(3)实验室要制取较多量的二氧化碳,装配气体发生装置时,应选择的仪器是DGH,可以随时添加药品。把制取二氧化碳结束后的废液未经处理直接倒入下水道,可能造成的危害是腐蚀铁质下水管道或污染水源等,不可随意排放。(4) 利用下图装置进行实验。①左管燃烧匙装有足量的锌粒,右管盛有稀硫酸,打开K1、K2反应发生,方程式是Zn+ H2SO4 = ZnSO4 +H2↑,该装置的优点是控制反应的发生和停止。为使反应停止,操作是关闭K1,容器内气压增大,使两药品分离,反应停止。②左管燃烧匙装有足量的白磷,右管盛水,光照引燃白磷,待白磷熄灭,冷却后,打开K2,右管液面下降,原因是白磷消耗氧气,玻璃管内压强减少。至液面不在下降,右管液面高度为h1,计算空气中氧气体积分数的表达式为(h0-h1)/h0 ×100%。
点睛∶根据反应物状态和反应条件选择气体制取装置,根据生成物气体的溶解性和密度选择气体的收集方法。
-
科目: 来源: 题型:
查看答案和解析>>【题目】控制变量法是实验探究的重要方法.利用如图所示的实验不能实现的探究目的是( )
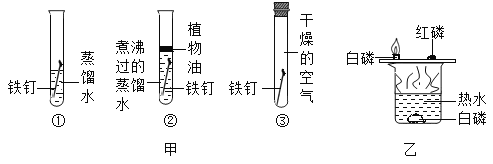
A.甲图中①②对比可探究铁的锈蚀与植物油是否有关
B.甲图中①③对比可探究铁的锈蚀与水是否有关
C.乙可探究可燃物的燃烧是否需要达到一定温度
D.乙可探究可燃物的燃烧是否需要与氧气接触
-
科目: 来源: 题型:
查看答案和解析>>【题目】(7分)四氧化三铁可用于医疗器械、电子等工业。某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验。
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表所示。
Zn(OH)2
Fe(OH)2
Mg(OH)2
开始沉淀的pH
5.7
7.6
10.4
沉淀完全的pH
8.0
9.6
12.4
(2)25℃时,Zn(OH)2可溶于pH>10.5的碱溶液。
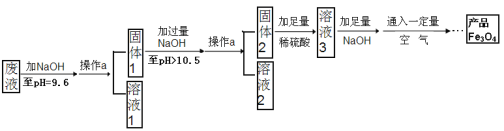
(3)制备Fe3O4的实验流程如下:
【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为 (写出其中一个)。
(2)操作a的名称为 。该操作需要的玻璃仪器有烧杯、玻璃棒、 等。玻璃棒在此操作中的主要作用是 。
(3)溶液1所含溶质有 (至少写两种成分的化学式);溶液3所含溶质的主要成分为 (写名称)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图甲、乙两种物质(不含结晶水)的溶解度曲线。下列有关说法正确的是( )
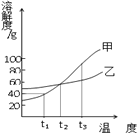
A. t2℃时,甲、乙溶液中溶质的质量分数一定相等
B. t1℃时,甲的溶解度为40
C. t3℃时,甲、乙的饱和溶液分别恒温蒸发相同的水,甲析出的晶体的质量比乙多
D. 甲的溶解度大于乙的溶解度
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知A~F是初中化学常见的含有氧元素的物质,其中A、B、C、D、E的物质类别不同,C、D、F的溶液能使无色酚酞溶液变色,B的固体常用于人工降雨,D广泛用于玻璃、造纸和洗涤剂的生产。如图是这些物质的转化关系,“→”表示物质间存在转化关系,“—”表示物质间能发生反应。请回答下列问题。
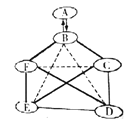
(1)(写化学式)A为__________,B为___________
(2)C和D反应的化学方程式为_________________ E和F反应的化学方程式为___________________________
(3)虚线间两物质间存在相互转化关系的是_________(填化学式)
-
科目: 来源: 题型:
查看答案和解析>>【题目】小维与家人聚餐时,对火锅燃料“固体酒精”产生了好奇,于是他与同学对其成分进行如下探究。
(查阅资料)(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的。
(2)氯化钙、氯化钡溶液均呈中性。
(提出问题)(1)酒精中是否含有碳元素?(2)固体酒精中氢氧化钠是否变质?
(作出猜想)猜想一:酒精中含有碳元素。猜想二:固体酒精中氢氧化钠已变质。
(实验探究)(1)如图1所示进行实验,发现_________________,可得出酒精中含有碳元素的结论。
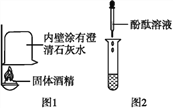
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现杯底有白色沉淀。取沉淀于试管中加入稀盐酸,现象为___________,化学方程式为____________________________。固体酒精中氢氧化钠已经变质。
(拓展延伸)为进一步确定固体酒精中是否还含有氢氧化钠,小维与同学继续探究。
(1)他另取少量固体酒精,加水溶解后,取上层清液,滴加酚酞溶液,现象是_____________,于是得出固体酒精中还含有氢氧化钠。
(2)小维的同学认为他的实验不能证明固体酒精中一定有氢氧化钠剩余,理由是____________。
(3)他们另取上层清液,加入足量的氯化钡溶液,充分反应后滴加氯化铁溶液,现象为________,他们一致认为固体酒精中氢氧化钠有剩余。
(反思交流)实验中,加入足量氯化钡溶液的目的是_________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】低钠盐适合患有高血压、肾病、心脏病的患者服用,苹果酸钠盐(C4H5O5Na)是低钠盐的一种。请回答:

(1)苹果酸钠盐口服液中含有的营养素有______种。每个苹果酸钠盐分子中共有_______个原子。
(2)苹果酸钠盐碳、氧元素质量比为 ______。
(3)若某病人每天食用4.68g苹果酸钠盐,则该病人每天最多吸收 ____g钠元素。
(4)药店销售一种苹果酸钠盐口服液,治疗效果非常好。该口服液的说明书如图,若某病人每天食用4.68g苹果酸钠盐,试计算该口服液中苹果酸钠盐的质量分数_________。
相关试题

