【题目】一种新型火箭推进剂在火箭发射过程中,发生反应的微观过程如下图所示。下列说法错误的是
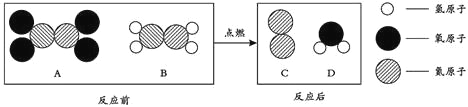
A. 上述四种物质中有两种氧化物 B. 氮元素在反应前后化合价一定发生了变化
C. 反应生成的C和D的质量比为14:9 D. A和B分子化学性质相同
参考答案:
【答案】CD
【解析】A、根据氧化物的定义分析可以看出,A、D属于氧化物,正确;
B、根据分析可以看出,C是氮气,属于单质,化合价为零,故氮元素在反应前后化合价一定发生了变化,正确;C、根据示意图可知,反应的化学方程式为:N2O4+2N2H4![]() 3N2+4H2O;所以生成C和D的质量比为:(14
3N2+4H2O;所以生成C和D的质量比为:(14![]() 6):(4
6):(4![]() 18)=7:6,错误;D、根据分析可以看出,分子A和分子B的分子构成不同,故二者的化学性质不同,错误。故选CD。
18)=7:6,错误;D、根据分析可以看出,分子A和分子B的分子构成不同,故二者的化学性质不同,错误。故选CD。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列实验常用仪器回答有关问题。

(1)仪器B的名称是__________。
(2)若用KMnO4加热制取氧气,发生装置应选用上述仪器中的_______________(填序号);其化学方程式为________;当用铁夹固定好试管后,要使试管口略低于试管底部,应调节螺旋________(填“K1”、“K2”或“K3”);要调节试管与酒精灯相对高度,应调节螺旋_______(填“K1”、“K2”或“K3”)。
(3)若用废铁片与稀盐酸反应制取氢气,并装配一个控制反应发生与停止的发生装置,应选上述仪器中________(填序号,下同)。若需测量收集到氢气的体积,则收集的仪器应选_________。
(4)图2为某同学制作的微型实验装置(夹持仪器略)。甲酸与热的浓硫酸反应的方程式为: HCOOH
 X+CO↑
X+CO↑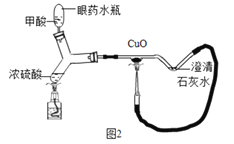
则X是__________(填化学式);
氧化铜的颜色变化为______________,其化学反应的方程式为_________。
此实验装置的主要优点是环保,其理由是___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~J是初中化学中常见的物质,它们之间有如图所示的转化关系(部分反应条件已略去)。其中A是一种液体,H是一种红色固体。已知在高温下单质碳能与多种金属氧化物反应生成金属单质和二氧化碳。请回答下列问题:
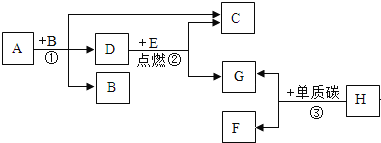
(1)写出下列物质的化学式:A_______G_________H________。
(2)E的组成元素一定含_____________,写出符合该条件的一种物质的化学式__________。
(3)反应①的化学方程式是______________;反应③的化学方程式是________________,基本反应类型_________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】黄铜(铜锌合金)是重要的金属材料,常用来制造机械零件,仪表和日用品。为测定黄铜材料中锌的含量,化学研究小组进行了实验:称取15.0g 此黄铜材料,向其中逐渐加入稀盐酸,测定产生气体的质量和加入稀盐酸的质量,并根据实验情况绘制了产生气体质量与加入稀盐酸的关系图。请你仔细分析此关系图,并进行计算:
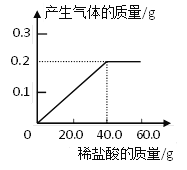
(1)15.0g黄铜材料中含锌___________g。
(2)稀盐酸中溶质的质量分数为__________(写出计算过程,下同。)
(3)当两者恰好完全反应时,求所得溶液的溶质质量分数为__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为 4NH3 + 3O2
 2X + 6H2O。下列说法中不正确的是
2X + 6H2O。下列说法中不正确的是A.氨气在常压下液化是物理变化 B.X的化学式为N2
C.液氨具有可燃性属于化学性质 D.液氨属于混合物
-
科目: 来源: 题型:
查看答案和解析>>【题目】在生产生活中,你会发现“化学就在身边”。
(1)洗洁精能清除油污,这是利用它的_____作用。
(2)上海世博园内安装的“直饮水”机,采用“活性炭+超滤层+紫外线”净水工艺。活性炭在此起__作用,净化后的水属于_____(选填“混合物”或“纯净物”)。
(3)在农业生产中,施用的草木灰(有效成份为K2CO3)属于_____肥。
(4)化学为体育不仅雪中送炭,而且锦上添花。举重、体操等项目的运动员在比赛前常用白色的“镁粉”搓手,这是因为“镁粉”质轻、吸水性好,可做防滑剂。“镁粉”的有效成份是碱式碳酸镁,它不可燃,300℃即分解,其分解的化学方程式是:Mg5(OH)2(CO3)4 △ 5MgO+X+4CO2↑,则X的化学式是_____;根据这些信息,还能推断出“镁粉”的另一种用途是_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(4分)下图是甲、乙、丙三种物质的溶解度曲线。
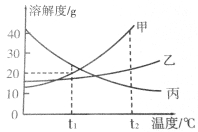
(1)t1℃时,三种物质的溶解度由小到大的顺序是 。
(2)t2℃时,要使用甲物质的饱和溶液变为不饱和溶液,可将溶液的温度 。
(3)t1℃时,将25g甲物质放入100g水中充分溶解。根据甲物质的溶解度曲线计算:未溶解的甲物质的质量是 g,所得溶液中溶质的质量分数是 。
相关试题

